2型糖尿病の発症において、インスリン抵抗性と並んで膵β細胞分泌不全の重要性が注目されています。近年、膵β細胞機能は、糖尿病発症の初期(正常耐糖能時)からすでに障害されていることが明らかとなってきました。インスリン分泌の障害とともに、膵β細胞量も2型糖尿病において減少していることは、多くの報告より確かなものとなってきましたが、糖尿病発症のどの段階で減少するのかについては、未だ不明な点が多いのが実情です。
私たちは、膵β細胞不全の発症過程における膵β細胞量減少のメカニズムの解明を主要な研究テーマとしています。
現在、私たちが取り組んでいる主な研究テーマは
- 膵β細胞におけるインスリンシグナル伝達経路の役割
- 膵β細胞不全における小胞体ストレスの関与に関する研究
- 膵β細胞不全発症におけるエピジェネティクスに関する研究
などです。
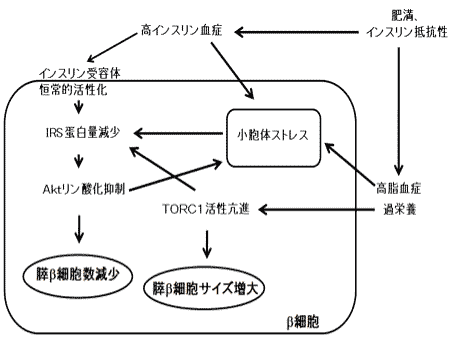
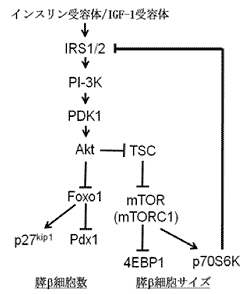 私たちは、これまでに膵β細胞におけるインスリンシグナルが膵β細胞量を調節する重要なシグナル伝達経路であり、このシグナルの減弱により膵β細胞量が減少し、膵β細胞不全が発症することを明らかにしました。また、膵β細胞の数とサイズのインスリンシグナルによる制御のメカニズムについても、左図のようなシグナル伝達経路をこれまでに報告してきました(Nat Genet. 2006;Mol Cell Biol. 2008)。
私たちは、これまでに膵β細胞におけるインスリンシグナルが膵β細胞量を調節する重要なシグナル伝達経路であり、このシグナルの減弱により膵β細胞量が減少し、膵β細胞不全が発症することを明らかにしました。また、膵β細胞の数とサイズのインスリンシグナルによる制御のメカニズムについても、左図のようなシグナル伝達経路をこれまでに報告してきました(Nat Genet. 2006;Mol Cell Biol. 2008)。
近年、糖尿病も小胞体ストレス関連疾患であることが示唆されるようになってきています。小胞体は、翻訳された蛋白の品質管理を行っていますが、インスリン分泌を行う膵β細胞は発達した小胞体を持っている一方で、さまざまな要因による小胞体ストレスに対し脆弱な組織であることが明らかとなってきています。私たちは、小胞体ストレスによって膵β細胞で発現誘導される転写因子C/EBPβを同定し、膵β細胞不全発症との関連を報告しました(J. Clin. Invest. 2010)。
これまでの疫学的研究によって、胎生期の環境が生活習慣病の発症に関与していることが明らかとなりつつあります。1986年以降Barkerらは、低体重出生児が将来的に耐糖能異常や高血圧を呈する確率が高いことを報告しており、こうした概念はDOHaD(Development origins of health and disease)と呼ばれ、さまざまな研究対象として関心が集まっています。
このような現象が起きるメカニズムとして、最近注目を集めているのがエピジェネティクス制御の関与です。遺伝学(ジェネティクス)がDNAの一時配列の変化によって次の世代に遺伝する変化を研究するのに対して、エピジェネティクスは「DNAメチル化やヒストン修飾などが関与するさまざまな生命現象」を対象にする分野です。
2型糖尿病患者では早期から膵β細胞量が減少していることが報告されており、高血糖を呈する以前に膵β細胞の脆弱性が既に存在していること、またそれが糖尿病発症の主要な原因であることが予想されています。現在、その膵β細胞の脆弱性にエピジェネティクスが重要な役割を果たしているのではないかと考え、研究を進めています(Biomed. Res. 2009)。
このように、インスリンシグナル、小胞体ストレス、エピジェネティクスの3つの視点より、膵β細胞不全のメカニズムを明らかにしようと解析を進めています。これらはそれぞれ独立した概念ではありますが、それぞれが密接に相互作用をしていることも明らかになりつつあります。さまざまなテーマが一つの真実に収束することを目標に研究を行っています。